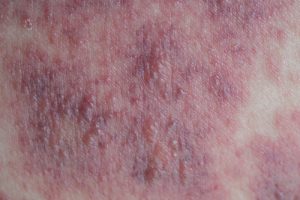
Presentati durante il 25° Congresso della European Academy of Dermatology and Venereology (EADV) i promettenti risultati degli studi di fase III LIBERTY AD SOLO 1 e SOLO 2 controllati rispetto al placebo, per dupilumab di Sanofi e Regeneron Pharmaceuticals, Inc. contro la dermatite atopica moderata e grave non corettamente controllata. I dati sono stati pubblicati sul New England Journal of Medicine (NEJM).
Dupilumab blocca le interleuchine 4 e 13, due citochine chiave nella risposta immunitaria di tipo 2 che si ritiene essere il principale fattore nella patogenesi della dermatite atopica e di altre patologie atopiche o allergiche, come asma e poliposi nasale. In queste ultime due indicazioni, dupilumab è al momento in sperimentazione in altri studi clinici.
“Questi risultati si aggiungono al crescente numero di dati a supporto di dupilumab come potenziale nuova opzione di trattamento per pazienti con dermatite atopica da moderata a grave che non riescono a controllare la malattia. I trial clinici di fase III, SOLO 1 e SOLO 2, sono i primi studi registrativi di ampia portata in cui una terapia sistemica sperimentale ha dimostrato di ridurre significativamente segni e sintomi della dermatite atopica e di migliorare alcuni indici della qualità di vita”, ha affermato Eric Simpson, medico dermatologo presso l’Oregon Health & Science University, e autore principale dell’articolo pubblicato sul NEJM. “Inoltre, la riduzione dell’intensità del prurito è importante perché il prurito è il sintomo più gravoso per i pazienti e ha un impatto su altri aspetti della loro vita, come il sonno”.
Nello specifico
A 16 settimane, il 37% dei pazienti adulti trattati con dupilumab 300mg una volta a settimana nello studio SOLO 1 e il 36% nello studio SOLO 2 hanno mostrato la pelle priva o quasi priva di lesioni, come misurato dalla scala IGA (Investigator’s Global Assessment), rispetto al 10% e 8% con placebo. Analogo risultato nel 38% dei pazienti adulti trattati con dupilumab 300mg ogni due settimane nello studio SOLO 1 e nel 36% nello studio SOLO 2. Inoltre, sempre a 16 settimane, negli studi SOLO 1 e SOLO 2 rispettivamente, il 52 e il 48% dei pazienti adulti trattati con dupilumab 300mg ogni settimana, e il 51 e il 44% dei pazienti adulti trattati con dupilumab 300mg ogni due settimane, hanno ottenuto una riduzione del 75% o superiore del punteggio EASI (Eczema Area and Severity Index), rispetto al 15 e al 12% del placebo.
Ancora, negli studi SOLO 1 e SOLO 2 rispettivamente, la percentuale di miglioramento del punteggio EASI dal basale è stata del 72 e del 69% nei pazienti trattati con il dosaggio settimanale a 300mg, e del 72 e del 67% nei pazienti trattati con la dose da 300mg ogni due settimane, rispetto a 38 e 31% con placebo. La riduzione dell’intensità quotidiana del prurito riportata dai pazienti, come misurata dalla scala NRS (Pruritus Numerical Rating Scale), era un endpoint secondario ed è stata raggiunta a 2, 4 e 16 settimane. La scala NRS va da 0 (nessun prurito) a 10 (il prurito più intenso possibile). Alla settimana 16, negli studi SOLO 1 e SOLO 2 rispettivamente, il 41 e il 36% dei pazienti trattati con dupilumab 300mg ogni due settimane, e il 40 e 39% dei pazienti trattati con dupilumab 300mg ogni settimana, hanno ottenuto una riduzione di 4 o più punti sulla scala NRS, rispetto al 12 e 10% con placebo.
La Food and Drug Administration (FDA) ha recentemente accettato la domanda di autorizzazione per i biologici (BLA – Biologics License Application) per dupilumab con revisione in via prioritaria. La data di riferimento per la decisione è il 29 marzo 2017. Nel 2014, l’FDA ha fornito a dupilumab la designazione di breakthrough therapy per il trattamento della dermatite atopica da moderata a grave, non controllata. Sia l’FDA sia l’EMA (European Medicines Agency) hanno accettato con riserva Dupixent® come nome commerciale per dupilumab.
Dupilumab è attualmente in sviluppo clinico; la sua sicurezza e la sua efficacia non sono state ancora completamente verificate da nessuna autorità regolatoria. Oltre alla dermatite atopica, il farmaco è in studio clinico nell’asma, nella poliposi nasale e nell’esofagite eosinofila. Una volta approvato, dupilumab sarà commercializzato da Regeneron e Sanofi Genzyme, la divisione di Sanofi specializzata in malattie rare, sclerosi multipla, oncologia e immunologia.