(Reuters Heath) – Mylan NV ha ottenuto l’ok dalla FDA per produrre il biosimilare di pegfilgrastim (Neulasta di Amgen). Mylan – in collaborazione con l’indiana Biocon – prevede di lanciare il farmaco, che si chiamerà Fulphila, nelle prossime settimane. Neulasta, usato per combattere le infezioni nei malati di cancro, ha portato l’anno scorso il fatturato di Amgen a 4,53 miliardi…
LeggiTag: Mylan
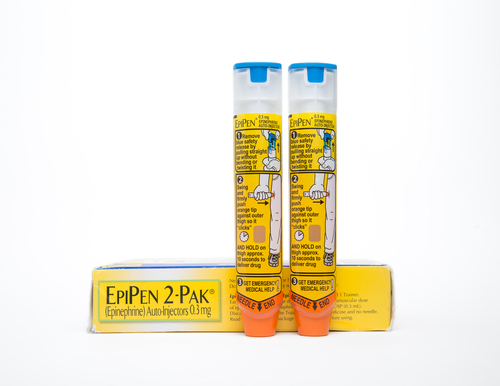
Mylan: problemi alla produzione di EpiPen. Si scaldano i concorrenti
(Reuters Health) – Rischio approvigionamento per EpiPen di Mylan e produttori europei di trattamenti di emergenza contro manifestazioni allergiche gravi intensificano la produzione di farmaci a base di adrenalina. Mylan ha iniziato ad avere problemi sulla fornitura di EpiPen due mesi fa in Gran Bretagna. Anche il Canada ha riscontrato problemi analoghi, mentre pochi giorni fa la Food and Drug…
LeggiMylan sugli OTC di Merck KGaA
(Reuters Health ) – Mylan sarebbe in una fase avanzata delle trattative per l’acquisto dell’unità di farmaci da banco di Merck KGgA, anche se la pharma americana produttrice di generici smentisce ufficialmente queste indiscrezioni, cosi come Merck KGaA. L’accordo, secondo alcune fonti, dovrebbe concludersi per una cifra compresa tra i 3,5 e i 4 miliardi di euro. L’azienda tedesca aveva annunciato…
LeggiMylan: accordo con Revance per biosimilare di Botox
(Reuters Health) – Mylan NV ha siglato un accordo di licenza con Revance Therapeutics Inc per sviluppare un biosimilare di Botox di blockbuster di Allergan. L’accordo prevede un pagamento anticipato di 25 milioni di dollari a Revance, ha detto Mylan. Il rivale di Revance contro Botox non è ancora stato approvato dalla Food and Drug Administration. La biotech ha riportato…
LeggiBiocon e Mylan: lettera richiamo FDA per sito produzione generico Lantus
Biocon e Mylan hanno ottenuto l’approvazione in Europa per il loro generico di Lantus, l’insulina di larghissimo successo prodotto da Sanofi. Adesso sperano di ottenere l’OK anche dalla FDA, ma c’è un ostacolo su questa strada. Biocon ha infatti annunciato oggi che la FDA ha inviato un modulo 483 contenente sei osservazioni emergenti dalla sua prima ispezione dell’impianto in cui…
LeggiMylan, il generico di Copaxone ruba quote di mercato a Teva
Il generico di Copaxone messo a punto da Mylan ha ottenuto l’approvazione della FDA solo tre mesi fa ma ha già mangiato una fetta considerevole della quota di mercato di Teva, produttore dell’originator. Secondo gli analisti di Credit Suisse, Mylan può contare sul 10% delle prescrizioni totali. Copaxone a lunga durata d’azione è fermo alla quota del 72%, mentre la…
LeggiMylan: al via studio per biosimilare Eylea (Regeneron)
(Reuters Health) – Mylan e Momenta Pharmaceuticals sono in procinto di dar vita a uno studio clinico per realizzare il biosimilare di Eylea, farmaco di successo per la degenerazione maculare prodotto da Regeneron. Il trial comincerà nella prima metà di quest’anno. In caso di successo, sarà probabilmente il primo biosimilare economico di Eylea. Regeneron afferma tuttavia di godere della protezione…
LeggiMylan/Biocon: FDA chiede chiarimenti su biosimilare di Neulasta (Amgen)
Cattive notizie per Biocon-Mylan, partner nella produzione di farmaci biosimilari per il mercato degli Stati Uniti. Dall’FDA è arrivata la richiesta di una Complete Response Letter (CRL) legata a questioni relative alla produzione. Secondo quanto dichiarato dall’azienda indiana, la lettera sembra essere rivolta alla produzione del biosimilare pegfilgrastim, copia del chemioterapico Neulasta di Amgen. Biocon, che ha offerto piena collaborazione, ha…
LeggiMylan: FDA dà il via libera a generico Copaxone. E Teva protesta
La FDA ha approvato la copia prodotta da Mylan di Copaxone, sia da 20 che da 40 mg, farmaco di punta dell’israeliana Teva. Teva, da parte sua, ha sottolineato in una dichiarazione che “qualsiasi lancio da parte di Mylan di una versione generica di Copaxone da 40 mg prima della decisione definitiva subordinata ai ricorsi sui brevetti pendenti in appello,…
LeggiMylan, Aurobindo e Fondazione Gates: arriva farmaco innovativo HIV in Africa
(Reuters Health) – Mylan e Aurobindo – due pharma specializzate nei generici – produrranno milioni di pillole destinate all’Africa contenenti dolutegravir, un inibitore dell’integrasi che evita il fenomeno della resistenza nei confronti della terapia standard. Grazie alla Fondazione Bill e Melinda Gates – che garantirà i volumi minimi di vendita dei farmaci – i costi annuali per la terapia non…
LeggiMylan: problemi per EpiPen, interviene FDA
(Reuters Health) – La FDA ha inviato una lettera di avvertimento a Meridian Medical Technologies, la divisione di Pfizer che produce, per conto di Mylan, il dispositivo di auto-iniezione salvavita in caso di shock anafilattico EpiPen. Secondo l’ente regolatorio americano, danni ai componenti sarebbero stati associati a effetti collaterali gravi e alla morte di alcuni pazienti. Già a marzo erano…
LeggiMylan e Biocon: FDA rinvia al 3 dicembre decisione su biosimilare Herceptin (Roche)
Mylan e Biocon devono attendere ancora tre mesi per conoscere la decisione della FDA in merito al biosimilare di trastuzumab che hanno messo a punto. Le due aziende avevano già incontrato difficoltà regolatorie nel richedere il via libera all’EMA. Secondo Biocon il rinvio della data di decisione della FDA è legato al’esame di chiarimenti richiesti nell’ambito del processo di candidatura.…
LeggiMylan, azionisti insoddisfatti. Ma la crescita è a due cifre
Dal 2011 Mylan gode di agevolazioni fiscali perché possiede impianti che trattano il carbone al fine di ridurre le emissioni inquinanti. Una riduzione che, secondo alcune fonti di stampa USA, avrebbe consentito all’azienda do aumentare i suoi guadagni, con crediti d’impresa pari a 95 milioni di dollari nel 2014, saliti poi a 100 nel 2015 e nel 2016, pari complessivamente…
LeggiMylan, Governo USA: EpiPen pagato il triplo
(Reuters Health) – Il Governo degli Stati Uniti potrebbe aver pagato fino a 1,27 miliardi di dollari in più per EpiPen, il farmaco di Mylan per il trattamento dello shock anafilattico. A calcolarlo è stato il Department of Health and Human Services americano. La cifra sarebbe pari a tre volte quanto proposto come risarcimento a ottobre dall’azienda farmaceutica americana. In risposta al…
LeggiMylan alza la voce contro FDA, che non approva generico di Advair
(Reuters Health) – La FDA non approva ancora il generico di Advair (GSK) e Mylan alza la voce. Il presidente della pharma americana, Rajiv Malik, ha affermato di non ritenersi obbligato a rispettare le norme contenute nel protocollo preparato dalla FDA. Una portavoce dell’agenzia regolatoria statunitense ha rifiutato di commentare la vicenda, dicendo che è proibito dalla legge discutere di…
LeggiMylan: studio clinico riaccende la polemica su EpiPen
Reuters Health) – Anche se è scaduto, EpiPen – l’autoiniettore di epinefrina di Mylan da utilizzare in caso di shock anafilattico – continuerebbe ad erogare alti livelli di sostanza, fino a quattro anni dopo la data indicata sulla confezione. A dimostrarlo è stato uno studio guidato da Lee Cantrell, che coordina il California Poison Control System di San Diego. La ricerca è…
Leggi