Doppio riconoscimento per nivolumab, farmaco immunoterapico di Bristol Myers Squibb. L’AIFA ha esteso la rimborsabilità di nivolumab in monoterapia per il trattamento adiuvante di adulti con melanoma allo stadio IIB o IIC sottoposti a resezione completa. Il via libera arriva sulla base dei risultati dello studio CheckMate -76k, in cui nivolumab ha dimostrato un beneficio a lungo termine nel trattamento…
LeggiTag: Bms
BMS: Commissione Europea approva liso-cel nel trattamento del linfoma follicolare
La Commissione Europea ha approvato la terapia CAR-T liso-cel (Breyanzi) di Bristol Myers Squibb per il trattamento di pazienti adulti con linfoma follicolare (FL) recidivante o refrattario, dopo due o più linee di terapia sistemica. In Italia liso-cel è già approvata e rimborsabile per l’uso nei pazienti adulti con linfoma diffuso a grandi cellule B (DLBCL), linfoma primitivo del mediastino…
LeggiBMS acquisisce spin off di bluebird bio
2seventy bio, spin off di bluebird bio focalizzata sulle terapie cellulari, entra a far parte di Bristol Myers Squibb. Secondo i termini dell’accordo siglato lunedì 10 marzo, BMS verserà 286 milioni di dollari per il capitale azionario di 2seventy bio, con una valutazione di 5 dollari ad azione. L’accordo consegna a BMS tutti diritti su idecabtagene vicleucel (Abecma), terapia cellulare…
LeggiBMS: ok CE a combo nivolumab/ipilimumab come terapia di prima linea nell’HCC
La Commissione Europea ha approvato la combinazione nivolumab/ipilimumab (Opdivo e Yervoy, di Bristol Myers Squibb), come trattamento di prima linea per adulti con carcinoma epatocellulare (HCC) non resecabile o avanzato. Questa approvazione si estende a tutti i 27 stati membri dell’Unione Europea e a Liechtenstein, Norvegia e Islanda. La decisione della Commissione Europea si basa sui risultati positivi dello studio…
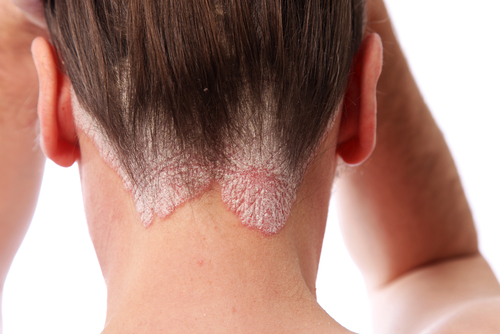
LeggiBMS lancia “Psorridi”, campagna digitale di sensibilizzazione sulla psoriasi
In Italia oltre un milione e mezzo di persone sono affette da psoriasi. La stragrande maggioranza – il 90% – soffre della forma “a placche”, detta così perché caratterizzata da placche rotonde od ovali, ben delineate e generalmente ricoperte da squame biancastre. Una condizione che ha un forte impatto sul benessere emotivo dei pazienti, influenzando le relazioni personali e professionali…
LeggiBMS: accordo miliardario con Prime per sviluppare terapie a base di cellule T
Bristol Myers Squibb ha concluso un accordo di ricerca e di licenza con la biotech USA Prime Medicine per lo sviluppo di terapie ex vivo con cellule T. I termini dell’accordo prevedono che Prime Medicine realizzi reagenti per l’editing genetico basati sulla tecnologia proprietaria PASSIGE. BMS, successivamente, li utilizzerà per sviluppare terapie ex vivo con cellule T. Prime Medicine riceverà…
LeggiBMS: la FDA approva Cobenfy, nuovo trattamento per la schizofrenia dopo 30 anni
La FDA ha approvato Cobenfy (xanomelina e cloruro di trospio) per la terapia della schizofrenia negli adulti. Dopo oltre 30 anni, per questa patologia è disponibile un farmaco completamente nuovo, “che ha il potenziale per cambiare il paradigma di trattamento”, sottolinea Chris Boerner, CEO di Bristol Myers Squibb. Cobenfy è un agonista muscarinico orale che ha come bersaglio i recettori…
LeggiCardiomiopatia Ipertrofica Ostruttiva. Al via da Milano la campagna ‘Fai posto al cuore’
Una panchina a forma di foglio diventa un simbolo per informare su una malattia cardiaca poco conosciuta. La nuova campagna nazionale che prende il via oggi si chiama “Fai posto al cuore” e ha l’obiettivo di sensibilizzare il grande pubblico sulla Cardiomiopatia Ipertrofica Ostruttiva (CMIO) e dare un messaggio di speranza ai pazienti che ne sono affetti. Si tratta di…
LeggiBMS: AIFA approva rimborsabilità di deucravacitinib nella psoriasi a placche da moderata a severa
L’Agenzia Italiana del Farmaco ha approvato la rimborsabilità di deucravacitinib per il trattamento della psoriasi a placche da moderata a severa. La decisione dell’AIFA fa seguito a quella analoga del 2023 dell’EMA. Deucravacitinib è un farmaco first-in-class inibitore orale della tirosin-chinasi 2 (TYK2) ed è il primo di una nuova classe di “piccole molecole”. Agisce selettivamente sul TYK2, inibendo la…
LeggiBMS, da CHECKMATE-067 risultati eccellenti a lungo termine per la combo Opdivo-Yervoy nel melanoma
I nuovi dati dello studio clinico CHECKMATE-067 mostrano come le persone affette da melanoma avanzato trattate con nivolumab (Opdivo) e ipilimumab (Yervoy) di Bristol Myers Squibb abbiano vissuto, in media, sei anni dopo la terapia. Prima dell’arrivo della combinazione di questi due farmaci, i pazienti con malattia avanzata sopravvivevano in genere solo sei-nove mesi dopo la diagnosi. I dati dello…
LeggiBMS, il Q2 si chiude con un fatturato di 12,2 miliardi di dollari
Il fatturato Q2 di BMS supera le aspettative e raggiunge i 12,2 miliardi di dollari, crescendo del 9% rispetto al 2023. A seguito di questi risultati, superiori alle attese, BMS ha alzato la propria guidance sugli utili rettificati per l’intero anno a un range compreso tra 0,60 e 0,90 dollari per azione. La precedente stima era di 0,40-0,70 dollari per…
LeggiBMS, Novartis e Roche: sclerosi multipla, un docufilm per raccontarla
Quattro storie per dare voce a chi ha incontrato sulla propria strada una patologia che cambia la vita: la sclerosi multipla. Quattro storie per raccontare a tutti che – nonostante tutto – è possibile continuare a condurre una vita normale, fare progetti, lavorare, avere figli. Questa, in poche battute, la sinossi di “Fra Destino e Libertà: il mio volo al…
LeggiEisai e Bristol Myers Squibb, stop all’accordo per sviluppo ADC
Eisai e Bristol Myers Squibb non collaboreranno più sviluppo e alla commercializzazione del coniugato anticorpo-farmaco farletuzumab ecteribulina (FZEC). Termina quindi l’accordo che le due aziende avevano firmato nel 2021. FZEC è un ADC mirato al recettore dei folati alfa (FRα). Eisai deterrà ora i diritti completi su FZEC e gestirà in modo indipendente lo sviluppo e la commercializzazione di questo…
LeggiBMS, da AIFA semaforo verde per le terapie CAR T ide-cel e liso-cel
L’Agenzia Italiana del Farmaco (AIFA) ha approvato la rimborsabilità della prima e unica terapia cellulare con CAR T, idecabtagene vicleucel (ide-cel), nel trattamento del mieloma multiplo, un tumore del sangue che ha origine nel midollo osseo. L’indicazione riguarda i pazienti adulti con malattia recidivante e refrattaria che abbiano già ricevuto almeno tre precedenti terapie, inclusi un agente immunomodulatore, un inibitore…
LeggiBoerner (CEO BMS): vogliamo ancora investire in M&A
Bristol Myers Squibb, reduce da una serie di acquisizioni sequenziali nel 2023, ha ancora liquidità da investire in operazioni di M&A. Lo ha dichiarato il CEO Christopher Boerner in occasione dell’incontro con gli investitori che si è tenuto questa settimana alla Global Healthcare Conference 2024 di Goldman Sachs. Le operazioni del 2023 di BMS sono state tutte di alto profilo,…
LeggiBMS, dall’ASCO lo stato dell’arte di nivolumab nel NSCLC di stadio precoce e avanzato
Bristol Myers Squibb ha reso noti i risultati delle analisi aggiornate degli studi CheckMate -77T, CheckMate -816 e CheckMate -9LA che supportano l’uso di nivolumab e delle sue combinazioni nel carcinoma polmonare non a piccole cellule (NSCLC) di stadio precoce e avanzato. Questi dati sono stati presentati al congresso annuale 2024 dell’American Society of Clinical Oncology (ASCO), che si è…
Leggi