L’Italia e’ seconda solo alla Gran Bretagna per i tempi medi totali che intercorrono tra l’autorizzazione del medicinale e la sua disponibilita’ sul territorio nazionale. Lo afferma l’Aifa sul proprio sito, citando i dati IMS Health riferiti all’anno 2014. Ad allungare i tempi tra l’approvazione da parte dell’Aifa e l’effettiva disponibilita’ per tutti i pazienti e’ la necessita’ da parte delle Regioni di inserire i nuovi farmaci nei prontuari regionali, un processo che per alcune richiede anni.
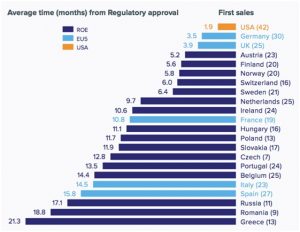
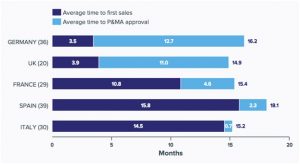
L’Italia, scrive l’agenzia, si piazza al diciottesimo posto (su 22 Paesi), per tempi medi d’accesso del farmaco al mercato dopo l’approvazione regolatoria (14 mesi e mezzo). Solo Grecia,Romania, Russia e Spagna registrano tempi piu’ lunghi. Se si considera tuttavia il tempo medio per l’autorizzazione alla commercializzazione e per le decisioni finali sul prezzo, l’Italia e’ il Paese degli EU5 con i tempi medi piu’ bassi (0,7 contro il 2,3 della Spagna, il 4,6 della Francia, l’11 del Regno Unito e il 12,7 della Germania) e grazie a questa performance si colloca al secondo posto dopo il Regno Unito per i tempi medi totali che intercorrono tra l’autorizzazione del medicinale e la sua disponibilita’ sul territorio nazionale a conclusione dell’iter negoziale e del processo di definizione del regime di rimborsabilita’. “Sono dati – sottolinea la nota – che smentiscono la vulgata secondo cui in Italia il percorso autorizzativo e negoziale sarebbe eccessivamente lungo e costituirebbe una barriera all’accesso tempestivo ai nuovi farmaci per i pazienti, confermando al contrario la validita’ dell’intuizione di affidare a un ente unico l’intero processo decisionale”.
AVERAGE TIME FROM REGULATORY APPROVAL TO FIRST SALES – PRODUCTS WITH FIRST SALES IN 2014
AVERAGE TIME FROM REGULATORY APPROVAL TO FIRST SALES AND FROM FIRST SALES TO NATIONAL P&MA APPROVAL IN 2014